摘要
基于薄膜梯度扩散(DGT)和平面光电极(PO)两种原位监测方法,首次从微米尺度获取了南四湖4个湖区泥-水界面(SWI)的活性磷以及亚铁(Fe2+)、亚硫(S2-)、pH和溶解氧(DO)等密切因子精细化分布变化信息, 并初步探讨了南四湖SWI活性磷变化特征与控制机制。结果直观揭示南四湖底泥剖面活性磷的浓度分布呈现明显的空间异质性,变化范围为0.34~2.36 mg/L,均值为1.26 mg/L。水平空间分布上独山湖((1.41±0.56) mg/L)和昭阳湖((1.97±0.42) mg/L)活性磷浓度显著高于南阳湖((1.07±0.20) mg/L)和微山湖((0.58±0.24) mg/L)。南四湖大部分采样点底泥中的活性磷与活性硫、活性铁浓度呈现正相关性,而昭阳湖活性磷、活性铁、活性硫浓度的相关性尤为显著(P<0.001),表明在剧烈有机质矿化过程中,活性硫可以通过与铁的相互作用促进活性磷的释放。SWI界面pH和DO结果显示受上游大量有机质输入的影响,底泥有机质降解消耗大量DO并产生大量S2-,硫酸盐还原占据主导地位,促进铁结合磷的释放。以上结果表明南四湖底泥中磷的形态转化受铁和硫两类氧化还原敏感元素控制,支持了磷、铁、硫的耦合释放机制,明确了硫与铁的生物地球化学循环共同控制泥中活性磷的释放。
Abstract
Herein the refined distribution of labile phosphorus (P) and its related factors, e.g. ferrous iron (Fe2+), sulfide (S2-), pH, and dissolved oxygen (DO) across the sediment-water interface (SWI) of Lake Nansi were simultaneously measured using two emergent in situ methods: diffusive gradient in thin films and planar optode. We further explored the characteristics and controlling mechanisms of labile P changes across the SWI of Lake Nansi. The distribution of labile P in the sediment profiles of Lake Nansi showed obvious spatial heterogeneity, ranging from 0.34 to 2.36 mg/L (average: 1.26 mg/L). The horizontal spatial distribution of labile P was significantly higher in Lake Dushan ((1.41±0.56) mg/L) and Lake Zhaoyang ((1.97±0.42) mg/L) than in Lake Nanyang ((1.07±0.20) mg/L) and Lake Weishan ((0.58±0.24) mg/L). The positive correlation between labile P and labile S, Fe in the sediment of most of the sampling sites in Lake Nansi was observed, particularly in Lake Nanyang (P<0.001), indicating labile S can promote P release through interaction with Fe during intense organic matter mineralization. 2D, high-resolution distribution of pH and DO indicated that the large amounts of organic matter from upstream affected the SWI, where the degradation of organic matter consumed large quantities of DO and produces large quantities of S2-, dominated by sulfate reduction, which promoted the release of Fe-bound P. The above results indicated that the migration of P in the sediment of Lake Nansi was controlled by two types of redox-sensitive elements, Fe and S, which supported the coupled release mechanism of P, Fe and S, and clarifies that the biogeochemical cycles of S and Fe jointly control the release of reactive P in the sediment.
Keywords
磷是控制水体初级生产力的决定因子,湖泊流域大面积外源磷输入极大加重了湖泊的富营养化和生态环境变化[1]。泥-水界面(SWI)是孔隙水和上覆水的过渡区,作为湖泊生态系统最重要界面之一,是控制磷等物质分配、输移、消减和转化等行为的关键带,几乎所有的水环境污染和生态分析问题均与SWI过程或效应有关。开展SWI磷的变化过程与机制研究对深入认识湖泊磷污染过程和控制措施具有重要意义。SWI发生着异常活跃的生物地球化学反应,显著影响溶解氧(DO)、pH、孔隙度、氧化还原电位等微环境特性,进而影响磷的迁移转化行为[2]。因此,准确获取SWI磷和界面微环境变化信息,将显著扩展内源磷污染发生过程与机制研究深度。
长期以来,微界面研究方法的不足制约了该领域研究深度的拓展。当前广泛采用异位分层-离心法或Peeper等监测手段,存在操作繁琐、界面破坏强、分辨率低等局限,极易导致所获取的泥-水剖面信息“失真”。而新进发展的梯度扩散薄膜技术(DGT)[3-4]和平面光电极技术(PO)[5]等原位技术以其操作简便、分辨率高、测量维度多等优势逐渐用于湖泊科学研究。DGT技术基于Fick定律[6],获得的活性物质形态主要包括游离的溶解态、不稳定无机络合态和不稳定有机络合形态,更好地反映水环境中物质的生物利用性。而PO技术基于荧光分析原理,利用数字成像技术拍摄目标物指示剂[7]发射荧光信息(强度[8-9]、寿命[10-11]、偏振等),进而获取pH、DO、温度等环境参数信息。当前两种技术多独立用于物质或环境因子的高分辨监测,如林建宇等[12]基于DGT技术原位获取了骆马湖SWI界面铁-磷-硫的同步变化信息,任静华等[13]基于PO技术获取了钝化土壤根际微界面pH和DO的同步变化信息。尽管PO和DGT检测目标上具有明显的互补性,但是当前鲜有研究将两者结合开展复杂SWI过程和机制的研究。
南四湖是我国北方最大的淡水湖,也是南水北调工程的重要调蓄湖泊。入湖河流上游长期接纳枣庄市、济宁市大部分生活及工业污水,湖泊年均总磷(TP)水平超过湖库Ⅲ类水质标准。当前对南四湖的研究多基于传统的磷形态分级方法获取不同磷形态分布变化信息,从较宏观尺度间接推测SWI界面磷的迁移转化机制,缺少SWI界面磷分布变化过程和机制研究[14-15]。本研究依托自主构建的PO和DGT两种原位高分辨监测技术,获取南四湖SWI活性磷及密切因子的同步精细化分布信息,进而从微观尺度揭示剖析南四湖内源磷污染状况及其迁移转化机制,为南四湖磷污染控制和水质管理提供参考依据。
1 材料与方法
1.1 研究区域概况
南四湖位于山东省和江苏省交界处,其南北长为120 km,东西宽为5~25 km,全湖面积为1266 km2,由北至南有4个相连的湖区,承载着调洪蓄水、南水北调、发展水产、航运交通等多方面重要功能。南四湖地势低洼,水源补给主要来自流域内的河川径流,还有部分引黄尾水注入南四湖,每到夏季汛期上游流域工业废水和生活污水经河流排入湖中[16]。
1.2 样品采集与处理
根据地理地貌、出入湖河流等差异在南四湖4个湖区南阳湖(NS1)、独山湖(NS2)、昭阳湖(NS3)、微山湖(NS4)各布设1个采样点(图1),于2023年4月采用重力式柱状采泥器(φ120 mm × 500 mm)采集包含原位界面上约20 cm高度的上覆水体和30~35 cm深度的泥柱芯,选择泥水界面清晰且无扰动的柱芯样品,封存避光带回实验室,随后将样品置于流动培养装置中,并设置与原位温度相近的条件进行48 h静态释放模拟培养,使其上覆水与底泥达到动态平衡后进行实验。
1.3 PO装置与现场应用
利用自制的便携式PO成像装置对现场采集的泥-水界面信息进行原位成像,该装置主要由激发光源、传感膜、光学信号采集(CCD/CMOS相机)及数据处理等主要模块组成(图2a)。其中采用自制多波段LED光源(389 nm、412 nm和 480 nm)作为激发光源,并使用Canon EOS 5 D 相机捕获荧光信号,参照文献[13]使用自制传感膜产生的荧光信号,同时在相机镜头前加装滤光片以消除其他波段荧光产生的干扰。采用8-羟基芘-1,3,6-三磺酸三钠盐(HPTS)染料和八乙基卟啉铂(PtOEP)两种染料制备pH和DO传感膜,详细步骤参考文献[13]。将传感膜裁剪成长方形(100 mm × 90 mm)后,使用黑色防水胶带将两种传感膜并排固定在有机玻璃窗口,投放至泥水界面上2~4 cm水界面下7~8 cm(图2a),并使用上述系统对pH和DO进行监测,进而捕获微米级SWI界面的pH和DO二维分布[13,17]。
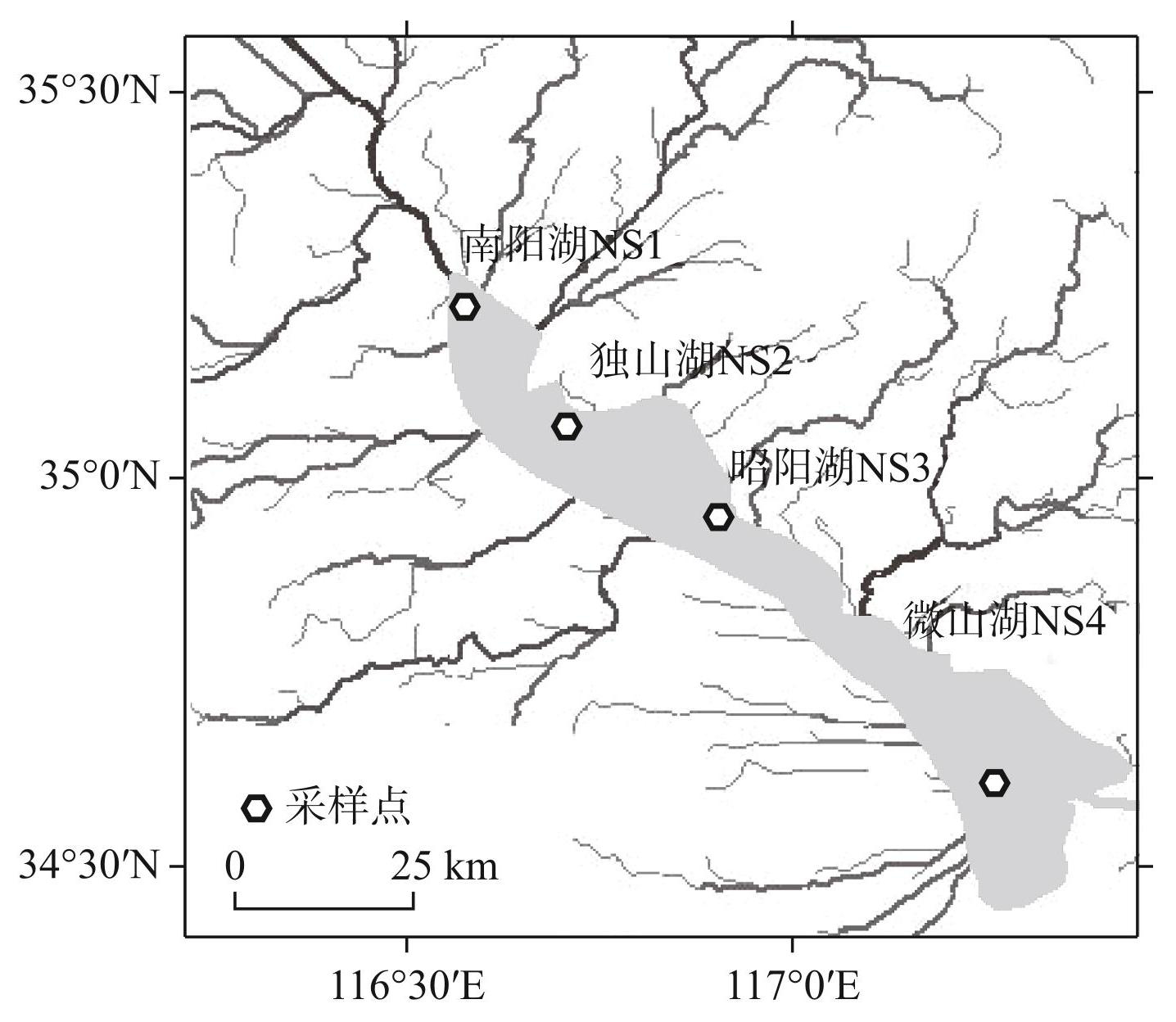
图1南四湖地理位置及采样点分布
Fig.1Location of Lake Nansi and distribution of sampling sites
1.4 DGT装置制备与应用
DGT装置由固定膜、扩散膜、滤膜、固定外壳载体4部分组成[18-20]。本研究以水合氧化锆(ZrOH)为吸附材料制备ZrOH DGT,用于磷的测定;以Chelex-100树脂和ZrOH为吸附材料制备Chelex-ZrOH DGT,用于磷和铁的一维同步测定;以碘化银(AgI)和ZrOH为吸附材料制备AgI DGT,用于硫的二维测定。3种固定膜和扩散膜的具体制备步骤可参考文献[21-23]。扩散膜参考Scally等[24]的方法以琼脂和水为材料制备。最后依次将Chelex-ZrOH、AgI、ZrOH的DGT固定膜、扩散膜和滤膜组装至ABS外壳中(南京维申)。
DGT装置参照林建宇等[12]的研究投放(图2b), 24 h后取出装置,拆解后用去离子水清洗掉表面泥颗粒,迅速装入湿润封口袋中冷藏保存。分析时,采用电脑密度成像计量(CID)技术[22]对AgI DGT和ZrOH DGT固定膜中的硫和磷进行二维成像分析(图2c);Chelex-ZrOH DGT固定膜经切片并提取后,分别使用酶标仪通过(Epoch)邻菲罗啉比色法和钼蓝比色法测定提取液中的Fe(II)和磷(图2d)。应用以上不同类型的DGT装置测定水体和底泥中能被生物利用物质的浓度(有效浓度),包括游离的溶解态、不稳定无机络合态和不稳定有机络合形态的活性铁(labile-Fe)、活性磷(labile-P)和活性硫(labile-S)[18]。
1.5 数据处理
1.5.1 DGT测定浓度和通量计算
DGT 提取活性磷和铁的一维数据通过Excel处理后使用Origin 2021 pro进行绘图,DGT使用电脑密度成像获得的磷和硫的二维数据采用Python 3.11进行处理及绘图。
Chelex-ZrOH DGT固定膜中活性磷、铁浓度CDGT(mg/L)由式(1)计算获得:
(1)
式中,M为DGT中目标分析物的累积量,mg;Δg为扩散膜和滤膜的总厚度,cm;D为目标物质在扩散膜中的扩散系数,cm2/s;A为DGT装置的窗口面积,cm2;T为放置时间,s。
Chelex-ZrOH DGT固定膜中目标离子积累量(M)一般经溶剂提取后由式(2)计算获得:
(2)
式中,ce为提取液浓度,Ve为提取剂体积,Vg为固定膜体积,fe为提取剂对固定膜上目标离子的提取率[4]。
1.5.2 PO数据校准和处理
PO系统通过不同激发光条件下获得的荧光图像绿色通道的比值进行拟合对pH值进行定量,pH值由式(3)Boltzmann方程获得:

图2研究装置示意图
Fig.2Schematic drawing of the research set-up
(3)
式中,A1和A2为拟合常数,dx为斜率,pKa为响应曲线的拐点,RpH为传感膜对pH值的相应信号。
DO浓度由特定激发光下获得的荧光图像红色通道与蓝色通道之比基于式(4)Stern-Volmer方程的亮点模型拟合获得:
(4)
式中,α为非猝灭荧光染料常数;KSV为方程常数,对于特定的猝灭剂其值是固定的,但需要根据应用温度校正;R为氧气存在时的荧光强度;R0为零氧状态下的荧光强度值;[O2]则表示O2浓度。
1.5.3 统计分析
为解析泥中活性磷的垂向变化,计算其浓度的水平变化,并绘制不同深度活性磷和活性硫的分布图。同时,以相同方法处理底泥中 pH 和 DO 的垂向变化,并利用 SPSS 24 进行 Pearson 相关性分析,探讨 DGT 和 PO 获取的磷、铁、硫关系。
2 结果与分析
2.1 南四湖SWI活性磷精细化时空分布特征
图3从2D和1D尺度直观揭示了南四湖SWI活性磷的精细化分布变化信息。总体来看,4个点位SWI剖面活性磷垂向变化特征相同,即水体中活性磷浓度整体较低而且稳定,NS1~NS4点位水体中活性磷浓度分别为(0.53±0.19)、(0.45±0.05)、(0.53±0.08)、(0.11±0.05)mg/L。在泥中活性磷浓度整体呈现随着深度增加先逐渐升高后又略降低的趋势,其中SWI下6~10 cm是活性磷热点区域,在此区域活性磷的垂向浓度波动较大,具有明显的垂向空间异质性,尤其是在SWI附近波动异常明显,NS1~NS4底泥中活性磷的平均浓度分别为(1.07±0.20)、(1.41±0.56)、(1.97±0.42)、(0.58±0.24)mg/L。本研究结果与龚梦丹等[26]在鄱阳湖和洞庭湖(活性磷峰值分别为0.41和0.52 mg/L)、林建宇等[12]在骆马湖(活性磷平均浓度为0.15 mg/L)以及张海舟等[27]在楚科奇海获得的活性磷的垂向分布特征一致。
在空间地区分布上,南四湖各个湖区底泥中的活性磷浓度差异显著,其中位于西北部湖区的NS2、NS3点位底泥中活性磷浓度最高, NS1和东南部的NS4点位底泥中的活性磷浓度较低,其水平空间地区分布特征与郑烨等[28]、王志齐等[29]的研究结论相似。这主要是因为NS2点位位于水产养殖区附近,有机质输入量较高,而NS3点位附近水体重度富营养,南四湖水域中菹草为优势水生植物,在南阳湖(NS1)和微山湖(NS4)分布较多 [30],位于东南部的NS4点位所在湖区为南四湖水质最好的湖区。
如图3b所示, NS1和NS4点位底泥中的活性磷浓度较低, NS2和NS3点位底泥中的活性磷浓度明显高于另外两个点位,不同的是, NS2点位底泥中的活性磷在泥-水界面剖面下9 cm处达到峰值,然后随着深度的增加浓度迅速减少,而NS3点位底泥中的活性磷浓度在泥水界面下6~9 cm范围内处在较高水平,随后缓慢减少至剖面最下层。总体来说,随着深度的增加,活性磷浓度呈现在泥-水界面下先剧烈增加,然后趋于平稳或降低的趋势,这种分布趋势与在SWI处于较弱的物理和生物扰动状态下的典型分布类似[19],其中NS2点位底层底泥pH呈现中性偏碱性,在此条件下活性磷易被释放,而铁主要以Fe3+的形式存在并形成氢氧化物沉淀,此特征与图5中NS2底层铁的一维分布特征相对应。
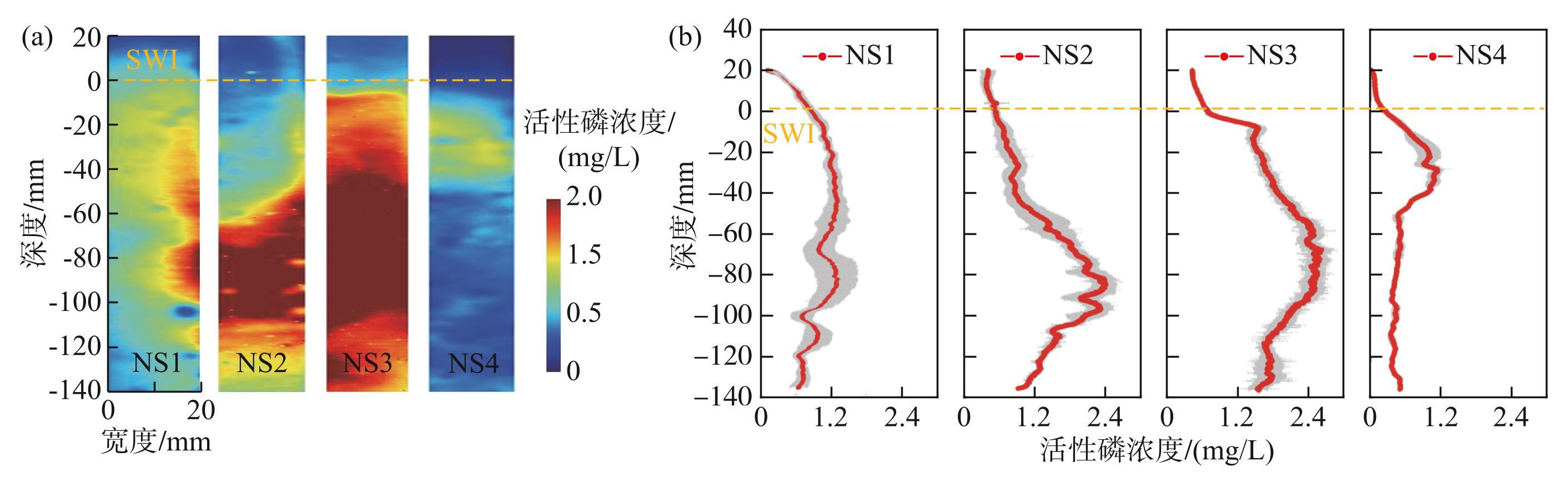
图3泥-水界面(SWI)剖面活性磷二维(a)和一维(b)分布
Fig.32D (a) and 1D (b) spatial distribution of labile P across the SWI
2.2 南四湖SWI微环境的分布特征
2.2.1 pH微环境变化特征
本研究获得了南四湖不同湖区SWI剖面pH的精细化分布特征,结果如图4所示,NS1、NS2、NS3和NS4点位上覆水pH分别为7.51±0.12、7.46±0.09、7.36±0.06和7.22±0.03,界面下底泥中pH 分别为7.31±0.04、7.38±0.07、7.33±0.09、7.17±0.11。通过pH的2D剖面图可直观地看出NS1、NS2和NS4点位上覆水中以及NS2和NS3点位底层底泥中的pH整体较高,4个点位的泥-水界面下2 cm范围内的pH较低。pH的1D剖面分布图可以明显看到NS1、NS2、NS4点位界面处pH骤减,NS3、NS4点位泥-水界面下pH随深度增加而逐渐升高。NS2和NS4点位的pH随沉积深度的增加而增加,反映了矿化作用程度的增加,有机碳的氧化分解使沉积环境的还原性增强,酸度减小,pH值增大[31]。
2.2.2 DO微环境变化特征
南四湖各湖区中NS1、NS2和NS4点位在SWI的DO精细分布特征如图4b所示。总体上分布特征相似,从PO二维成像结果可知,4个采样点界面以上的上覆水中DO浓度较高,界面上的DO浓度范围平均值为(111.40±27.37)、(106.26±12.82)、(19.66±7.01)、(88.11±44.87)μmol/L,而泥-水界面以下DO的平均浓度分布较均匀且水平较低,一维图像可观察到4个点位泥-水界面处DO浓度骤减,分别为(1.51±1.08)、(6.31±3.74)、(0.87±0.50)、(3.44±2.70)μmol/L。NS2点位附近菹草生长较为旺盛,水生植物的存在可能是造成本点位底泥DO浓度与其他点位出现差异的原因。
2.2.3 活性铁变化特征
底泥中活性铁浓度的波动范围较大,NS1~NS4点位分别为(0.20±0.09)、(0.64±0.34)、(0.21±0.11)和(0.57±0.15)mg/L;上覆水中活性铁浓度则较稳定,NS1~NS4点位分别为(0.19±0.09)、(0.11±0.04)、(0.08±0.03)和(0.13±0.08)mg/L。活性铁的剖面分布趋势与活性磷的分布特征相似,此分布特征与龚梦丹等的研究结果相同,均呈现在界面下0~6 cm先增加又缓慢降低的过程。NS2点位的活性铁浓度在界面附近有剧烈的升高, NS1和NS3点位的活性铁在底泥中的浓度水平较低,且垂向分布较稳定。NS2和NS4点位的活性铁浓度在界面处骤增,NS2点位在界面下6 cm骤降,NS4点位底泥中随着深度增加浓度逐渐升高。位于南四湖东南部的NS3和NS4点位中的低DO水平和高pH水平,分别对应NS3点位底泥中活性磷和NS4点位底泥中活性铁较高的活化释放效率,该现象支持了以往研究阐述的底泥中活性磷、铁的释放随着溶解氧的耗尽被激活,好氧条件有利于活性磷固定的结果[32-33]。
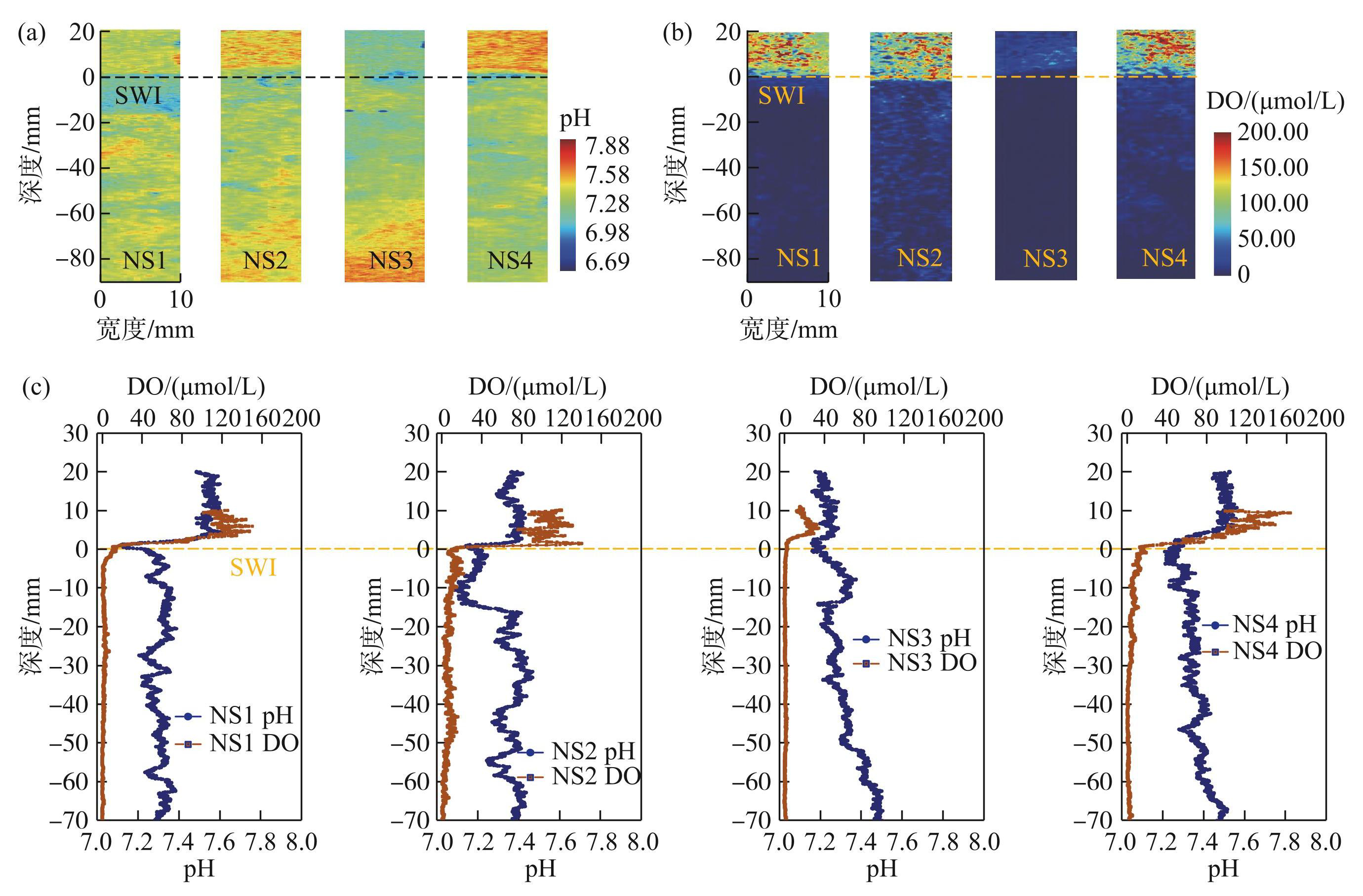
图4泥-水界面(SWI)剖面活性pH、DO二维(a、b)和一维(c)分布
Fig.42D (a, b) and 1D (c) spatial distribution of labile pH and DO across the SWI
2.2.4 活性硫变化特征
南四湖4个湖区泥-水界面活性硫的垂向分布趋势与活性铁有所不同,在界面以下的表层底泥中水平较低,而后随深度的增加含量有所上升。界面上2 cm处的活性硫含量较低且稳定,NS1~NS4点位平均浓度分别为(0.04±0.04)、(0.15±0.03)、0、0 mg/L,底泥中活性硫含量分别为(0.20±0.07)、(0.31±0.31)、(0.31±0.22)、(0.17±0.06)mg/L,底泥中的活性硫主要来源于有机质矿化过程[28,34]。南四湖底泥活性硫浓度略低于骆马湖[12]泥剖面活性硫的浓度(0.01~0.63 mg/L),但显著高于吴松峻等[35]获得的太湖西岸聚藻区底泥的硫酸盐平均浓度((0.12±0.01)mg/L)。
2.3 南四湖SWI活性磷的变化机制初探
2.3.1 微环境特征对活性磷迁移转化行为的影响
底泥磷的释放往往受多因素共同作用。本研究采用室内静态模拟实验,忽略了水力扰动等物理因素通过再悬浮作用、浓度梯度与扩散机制以及环境因子的综合作用产生的对底泥中活性磷释放的促进作用。在湖泊生态系统中,pH和DO是控制活性磷释放的关键因素。泥-水界面的DO浓度是影响铁氧化物对磷的吸附能力、有机质矿化速率以及微生物丰度和活性的重要因素[36]。DO通过调节泥水的氧化还原电位来控制内源磷的转化过程。南四湖NS1、NS2、NS4点位的DO浓度与活性磷释放均呈现显著负相关关系,r值分别为-0.817(P<0.01)、-0.435(P<0.01)、-0.524(P<0.01),支持了以往研究发现的在氧气充足的条件下,铁离子(Fe2+)在间隙水中氧化生成具有较大比表面积的铁氧化物,从而吸附可溶性无机磷,而在厌氧或缺氧条件下,铁氧化物被还原并将可溶性无机磷释放的理论。
而pH的变化影响铁的氧化还原状态和磷的溶解度,高pH条件下,生成的羟基离子与磷酸盐竞争吸附点,可能导致更多活性磷的释放,同时较低的pH水平可使铁氧化物溶解从而释放其结合的磷酸盐导致活性磷释放。本研究中NS1、NS2、NS4点位的pH水平与活性磷释放呈现显著相关性,其对应r值分别为-0.586(P<0.01)、0.851(P<0.01)、-0.693(P<0.01),获得的沉积物剖面整体pH水平随深度变化趋势与Fan等通过平面光电极获得的剖面变化趋势相同,即在有机质大量降解消耗溶解氧的还原区域,被铁氧化物固定的磷在还原条件下易因铁氧化物还原溶解被活化释放[37],同时随着有机碳分解、还原性增强,底泥环境中酸度减小,pH增大[31],而NS1、NS3点位出现的pH值热点区域可能是大型水生动物活动产生的沉积物空间异质性造成的[17,38]。因此,DO和pH的变化可直接影响湖泊底泥中活性磷的迁移转化行为,并控制其在水体中的分布和循环。
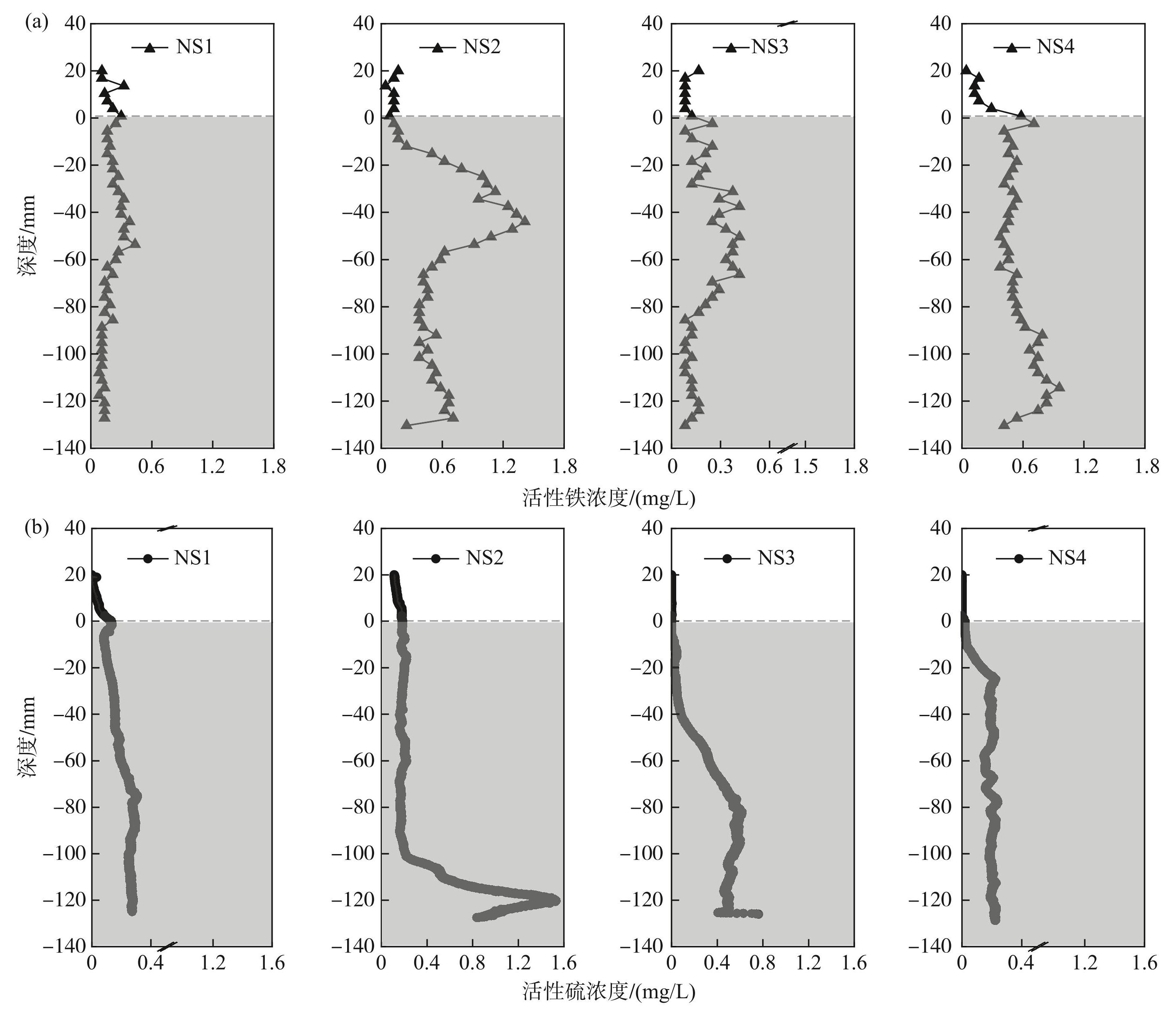
图5SWI剖面活性铁、硫的一维分布
Fig.51D spatial distribution of labile Fe and S across the SWI
2.3.2 活性铁、硫对活性磷迁移转化行为的影响
铁和硫是底泥中最普遍的氧化还原敏感元素。Han等[19]研究认为硫和铁的氧化还原循环过程对泥-水界面磷的释放和迁移具有重要的调控作用。南四湖中底泥的磷形态以无机磷为主[29],其中的活性组分主要为铁结合态磷。为深入探讨底泥磷、铁和硫三者的相互作用关系,对南四湖底泥活性磷、铁、硫剖面变化与浓度分布进行分析比较。结果表明NS1、NS3和NS4点位的活性磷与活性硫浓度均呈正相关(P<0.01),并且在NS3点位相关性尤为显著,r值分别为0.348、0.713、0.381,只有NS2点位几乎不相关(r=0.089);NS1、NS2和NS3 3个点位的活性磷浓度与活性铁浓度均呈正相关,r值分别为0.351(P<0.05)、0.447(P<0.01)、0.612(P<0.01),同时NS3点位的相关性仍较其他点位显著,而NS4点位的活性磷与活性铁浓度之间无相关性。Jensen等[39]对丹麦15个湖泊的底泥展开调查时发现底泥中总铁与总磷含量呈显著正相关,此外后续也有报道指出还原条件下,底泥中Fe3+还原为Fe2+,促使铁结合态磷解析形成有效态磷,并向孔隙水释放和向上覆水扩散,且磷、铁释放具有同步性[40]。为进一步探究湖泊中控制磷释放的机制,对南四湖底泥活性磷、铁、硫浓度分布结果进行比较(图6),发现NS1点位的活性磷、铁、硫均处于较低水平,同时具有低DO和低pH,这可能由于该采样点位于养殖鱼塘附近,大量有机质输入及分解过程导致底泥呈还原环境。NS4点位底泥pH和DO较高,同时活性磷和活性硫浓度相对较低,表明此处活性磷可能与铁氧化物结合,释放受到铁的抑制。在NS3点位,活性硫的含量较高,易与Fe2+结合形成黑色FeS沉淀,导致活性铁浓度显著降低(图6),这与现场观察到的底泥颜色偏深相一致。同时NS3点位底泥中DO浓度较低,且pH值较高,分析这一现象可能是由于水生植物较多,植物残体腐烂,产生厌氧微环境导致大量活性硫和活性磷的释放。Gunnar等[41]通过浓度梯度实验发现,溶液中的活性铁和磷的摩尔比(RFeP)超过2时,通过形成磷酸铁化合物降低活性磷的浓度。陈婷等[42]通过比较总结不同区域泥-水界面活性铁磷以及磷扩散通量的关系发现RFeP与磷扩散通量呈反比。对南四湖4个点位的RFeP进行计算,结果显示NS2和NS3点位的RFeP<2,为磷释放风险较高的两个湖区,且NS3点位的RFeP水平更低,对应底泥中的活性磷浓度更高。
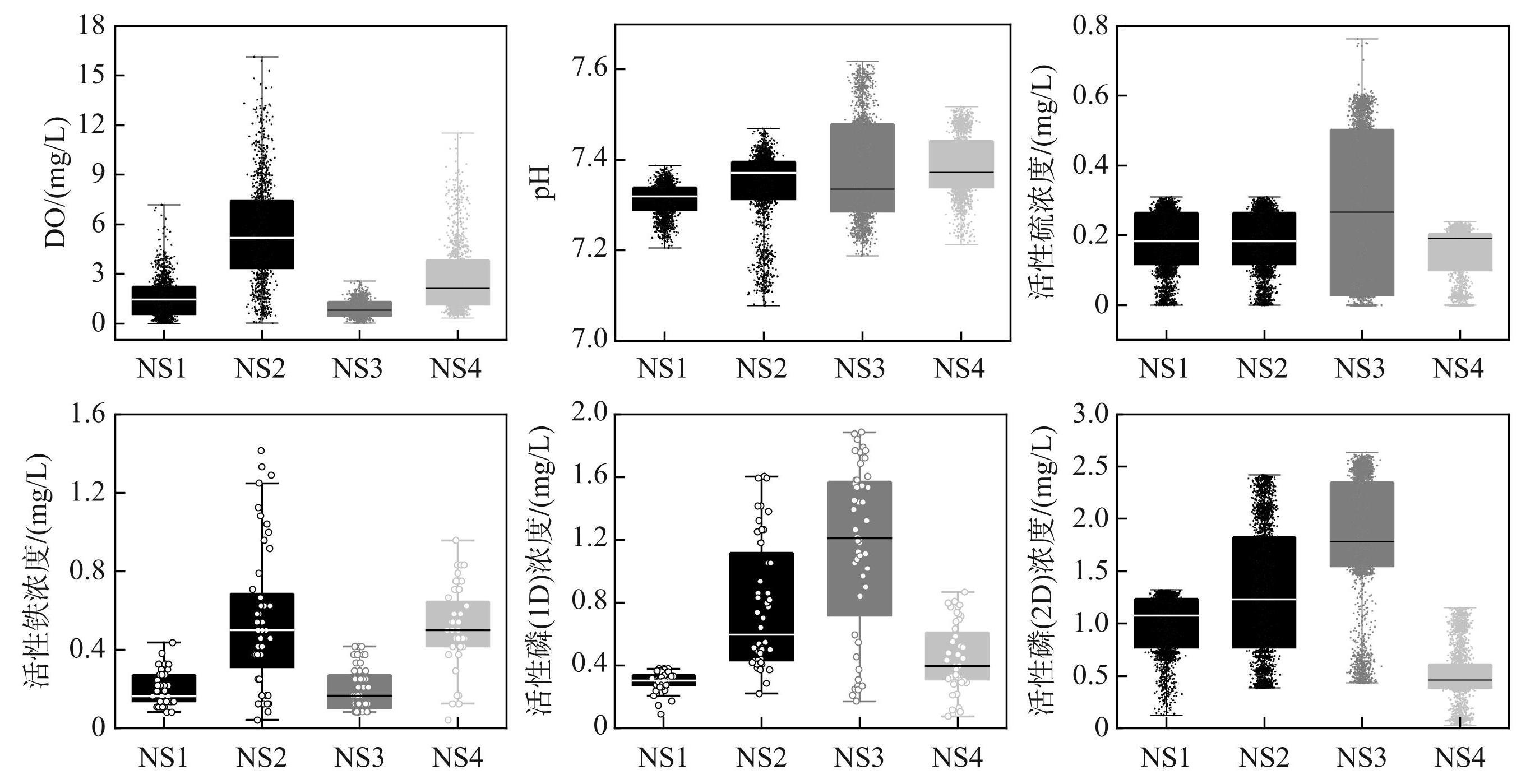
图6泥-水界面(SWI)剖面活性磷、铁、硫及pH、DO箱式图
Fig.6Box-plot of concentrations for labile P, Fe, S and pH, DO across the SWI
在不同的湖区中控制磷释放的机制有所不同,硫、铁的氧化还原循环过程在湖泊地球化学循环过程中具有重要作用[19,43]。湖泊底泥中的铁通常存在多种形态,其分布和形态特征受到底泥的化学环境影响。在氧化条件下,铁主要以铁氧化物或羟基化铁的形式存在,能有效吸附或结合磷等营养物质,以往研究表明缺氧条件下底泥中的Fe3+还原生成大量活性Fe2+,与图4b中的底泥极低的溶解氧含量相对应[44-45]。在氧化条件下,铁氧化物可与磷酸盐结合,从而促进磷酸盐的固定沉积过程,而铁化学还原过程以及由还原铁细菌主导的微生物铁还原过程则是磷的释放过程,由铁氧化还原反应控制的吸附解析过程是磷迁移的主要途径,二者构成了Fe-P循环。同时硫的氧化还原循环过程也会影响磷的迁移转化,在有机质矿化的过程中,硫酸盐与铁氧化物作为电子受体互相竞争[46-47],Fe3+将还原为Fe2+[43-46],并与硫酸盐还原产生的S2-形成共沉淀物FeS和FeS2,与此同时生成的H2S与磷酸铁发生置换反应释放出SO2-4,还原导致pH升高,OH-与PO3-4竞争吸附点位,促进活性磷的释放[48-49],这些过程可能导致铁结合磷的快速溶解,使水体富营养化加剧,并提供持续的厌氧条件,从而增加了磷释放的风险[50]。南四湖的大多数采样点的磷、硫之间以及硫、铁之间表现出正相关性,且在磷、铁相关性系数较高的NS3点位,其磷、硫也表现出较高的相关性,同时NS3点位的活性硫含量相比其他3个点位更高,代表着更活跃的有机质矿化过程,对应NS3点位的活性磷含量远高于其他3个点位,间接支持了活性硫可与铁的相互作用促进铁结合磷的释放的结论。此现象支持了以往研究中阐述的有机质矿化,硫酸盐还原从而促进活性磷释放的理论[46-49]。
3 结论
1)基于原位高分辨DGT技术首次获得南四湖SWI剖面活性磷的精细化分布信息,结果表明,底泥磷的空间分布具有明显的差异性。从地区分布上看,由于南四湖西北部靠近山东省济宁市区,受入湖河流影响,西北部NS1、NS2、 NS3点位的活性磷浓度((1.07±0.20)、(1.41±0.56)、(1.97±0.42)mg/L)较东南部NS4点位((0.58±0.24)mg/L)高。
2)基于PO技术获得的南四湖SWI剖面微环境分布显示,SWI界面上pH、DO微环境整体均匀分布,而在底泥剖面微环境具有明显的异质性,整体来看各点位pH和DO在界面处骤减,底泥的pH整体随深度增加缓慢增加,而DO随深度增加而减少。基于DGT技术获得的活性铁、硫分布显示,底泥中的铁大体呈现自界面向下先升高后降低的趋势,并在40~70 mm深度范围内出现峰值,活性硫浓度呈现随底泥深度增加而增大的趋势。
3)原位高分辨获取南四湖SWI活性磷及密切环境因子的同步精细化分布信息。结果表明,不同点位中磷释放机制存在差异,氧化还原条件和有机质输入均对P、Fe和S形态变化产生影响。相关性分析表明,NS1、NS3和NS4点位的活性P与活性S浓度均呈正相关(P<0.01);NS1、NS2和NS3点位的活性P、活性Fe浓度均呈正相关(P<0.05),其中NS3点位显示出P、S及Fe浓度的高度相关性,这一研究支持了Fe和S的氧化还原循环对P释放和迁移具有重要调控作用的理论。
